本文通過最淺顯易懂的方式解讀動力電池的相關(guān)概念、結(jié)構(gòu)及工作原理,讓大家對動力電池有更深入的理解。

一、若干重要概念
1、電壓(V)
①開路電壓:指電池在沒有連接外電路或者外負(fù)載時的電壓。開路電壓與電池的剩余能量有一定的聯(lián)系,電量顯示就是利用這個原理。
②工作電壓:是指電池在工作狀態(tài)下即電路中有電流流過時電池正負(fù)極之間的電勢差,又稱負(fù)載電壓。在電池放電工作狀態(tài)下,當(dāng)電流流過電池內(nèi)部時,必須克服內(nèi)阻的阻力,故工作電壓總是低于開路電壓。
③放電截止電壓:指電池充滿電后進(jìn)行放電,放完電時達(dá)到的電壓(若繼續(xù)放電則為過度放電,對電池的壽命和性能有損傷)。
④充電限制電壓:充電過程中由恒流變?yōu)楹銐撼潆姷碾妷骸?

電池充放電電壓變化曲線
2、電池容量(Ah)
①定義:電池容量是指電池所能夠儲存的電量多少,容量是電池電性能的重要指標(biāo),它由電極的活性物質(zhì)決定。
②單位:容量用C表示,單位用Ah(安時)或mAh(毫安時)表示。
③公式:C=It,即電池容量(Ah)=電流(A)x放電時間(h)。
④舉例:容量為10安時的電池,以5安培放電可放2小時,以10安培放電可放1小時。
⑤影響因素:電池的實際容量主要取決于以下幾個因素:活性物質(zhì)的數(shù)量、質(zhì)量,活性物質(zhì)的利用率。
⑥額定容量:在規(guī)定條件下測得的,由制造商給定的蓄電池容量。
⑦可用容量:在規(guī)定條件下,從完全充電的蓄電池中釋放的電量。
⑧理論容量:假設(shè)活性物質(zhì)完全被利用,蓄電池可釋放的容量。
3、電池能量(Wh)
①定義:指電池儲存的能量的多少,用Wh來表示
②公式:能量(Wh)=額定電壓(V)×工作電流(A)×工作時間(h)。
③舉例:3.2V15Ah單體電芯的能量為48Wh,3.2V100Ah電池組的能量為320Wh。

電池能量是衡量電池帶動設(shè)備做功的重要指標(biāo),容量不能決定做功的多少。
4、能量密度(Wh/Kg)
①定義:指單位體積或單位質(zhì)量所釋放的能量,通常用體積能量密度(Wh/L)或質(zhì)量能量密度(Wh/kg)表示。
②舉例:如一節(jié)鋰電池重325g,額定電壓為3.7V,容量為10Ah,則其能量密度為113Wh/kg,下表為理論值,在實際應(yīng)用情況中需要考慮電池結(jié)構(gòu)中的殼體、零件等各方面因素。
目前鋰電池的能量密度是鎳鎘和鎳氫電池的3和1.5倍,能量密度的高低是由材料密度與結(jié)構(gòu)決定的。

5、功率與功率密度
①功率是指在一定的放電制度下,單位時間內(nèi)電池輸出的能量,單位為W或kW。
②功率密度又稱比功率,是單位質(zhì)量或單位體積電池輸出的功率,單位為W/kg或W/L。
比功率是評價電池及電池包是否滿足電動汽車加速和爬坡能力的重要指標(biāo)。
6、放電倍率(A)
①定義:放電倍率是指在規(guī)定時間內(nèi)放出其額定容量(C)時所需要的電流值,它在數(shù)值上等于電池額定容量的倍數(shù)。
②舉例:以10Ah電池舉例,以2A放電,則放電倍率為0.2C,以20A放電,則放電倍率為2C。
7、充電方式

①CC/CV:CC即恒流,以固定的電流對電池充電;CV即恒壓,以固定的電壓對電池充電,充電電流會隨著電池充滿逐漸下降。
②涓流充電:指以小于0.1C電流對電池充電,一般在電池接近充滿電時,迚行補充充電時采用,若電池對充電時間沒有嚴(yán)格要求的話,建議采用涓流充電方式充電。
③浮充電:隨時對蓄電池用恒壓充電,使其保持一定的荷電狀態(tài)。

8、充、放電深度(SOC DOD):電池保有容量數(shù)值的表示方法。
①荷電狀態(tài)state-of-charge(SOC):蓄電池放電后剩余容量與全荷電容量的百分比。
②放電深度depth ofdischarge(DOD):表示蓄電池放電狀態(tài)的參數(shù),等于實際放電容量與額定容量的百分比。
③深度放電deep discharge:表示蓄電50%或更大的容量被釋放的程度。
④舉例:充、放電深度以百分比率來表示,如:容量為10Ah的電池放電后容量變?yōu)?Ah,可以稱為80%DOD;容量為10Ah的電池,充電后容量為8Ah,80%SOC。形容滿充滿放,通常稱為100%DOD。

9、內(nèi)阻(m?)
①定義:電池的內(nèi)阻是指電池在工作時,電流流過電池內(nèi)部受到的阻力。內(nèi)阻大小主要受電池的材料、制造工藝、電池結(jié)構(gòu)等因素的影響。
②分類:電池內(nèi)阻包括歐姆內(nèi)阻和極化內(nèi)阻,歐姆內(nèi)阻是由電極材料、電解液、隔膜電阻及各部分零件的接觸電阻組成,極化內(nèi)阻包括電化學(xué)極化與濃差極化引起的電阻。
③影響因素:電池內(nèi)阻是一個非常復(fù)雜而又非常重要的特性,影響內(nèi)阻的因素有材料、結(jié)構(gòu)等。
④產(chǎn)生結(jié)果:由于內(nèi)阻的存在,當(dāng)電池放電時,電流經(jīng)過內(nèi)阻要產(chǎn)生熱量,消耗能量,電流越大,消耗能量越多,所以內(nèi)阻越小,電池的性能越好,不僅電池的實際工作電壓高,消耗在內(nèi)阻上的能量也少。

10、自放電率(%/月)
①定義:電池在儲存過程中,容量會逐漸下降,其減少的容量與電池容量的比例,稱為自放電率。
②原因:由于電極在電解液中的不穩(wěn)定性,電池的兩個電極發(fā)生了化學(xué)反應(yīng),活性物質(zhì)被消耗,轉(zhuǎn)為電能的化學(xué)能減少,電池容量下降。
③影響因素:環(huán)境溫度對其影響較大,過高溫度會加速電池的自放電
④表示:電池容量衰減(自放電率)的表達(dá)方法和單位為:%/月。
⑤產(chǎn)生結(jié)果:電池自放電將直接降低電池的容量,自放電率直接影響電池的儲存性能,自放電率越低,貯存性能越好。

11、循環(huán)壽命(次)
①定義:二次電池經(jīng)歷一次充放電稱為一個周期或一次循環(huán),電池在反復(fù)充放電后,容量會逐漸下降,在一定的放電條件下,電池容量降至80%時,電池所經(jīng)受的循環(huán)次數(shù)就是循環(huán)壽命。
②影響因素:不正確使用電池,電池材料,電解質(zhì)的組成和濃度,充放電倍率,放電深度(DOD%),溫度,制作工藝等都對電池的循環(huán)壽命有影響。

12、記憶效應(yīng)
①定義:電池的記憶效應(yīng)是指未完全放電的電池,在下一次充電時所能充電的百分比。
②原因:電池內(nèi)物質(zhì)產(chǎn)生結(jié)晶,如鎳鎘電池中,Cd不斷聚集成團形成大塊金屬鎘,降低了負(fù)極的活性。
③避免:為了消除電池的記憶效應(yīng),在充電之前,必須先完全放電,然后再充電。
鋰離子電池?zé)o記憶效應(yīng)。
13、放電平臺
指放電曲線中電壓基本保持水平的部分。放電平臺越高、越長、越平穩(wěn),電池的放電性能越好。
14、電池組的一致性
由多個單體電芯串連、并聯(lián)在一起就組成了電池組。電池組的整體性能和壽命取決于其中性能較差的一個電芯,這就要求電池組中每個電芯性能的一致性要高。除了單體電芯本身性能的誤差和原材料質(zhì)量的好壞,最主要原因是制造工藝,工藝的改進(jìn)對提高電池的質(zhì)量非常重要。
15、化成
電池制成后,通過一定的充放電方式將其內(nèi)部正負(fù)極活性物質(zhì)激活,改善電池的充放電性能及自放電、貯存等綜合性能的過程稱為化成。電池經(jīng)過化成后才能體現(xiàn)其真實的性能。同時化成過程中的分選過程能夠提高電池組的一致性,使最終電池組的性能提高。

二、鋰電池結(jié)構(gòu)與原理解讀
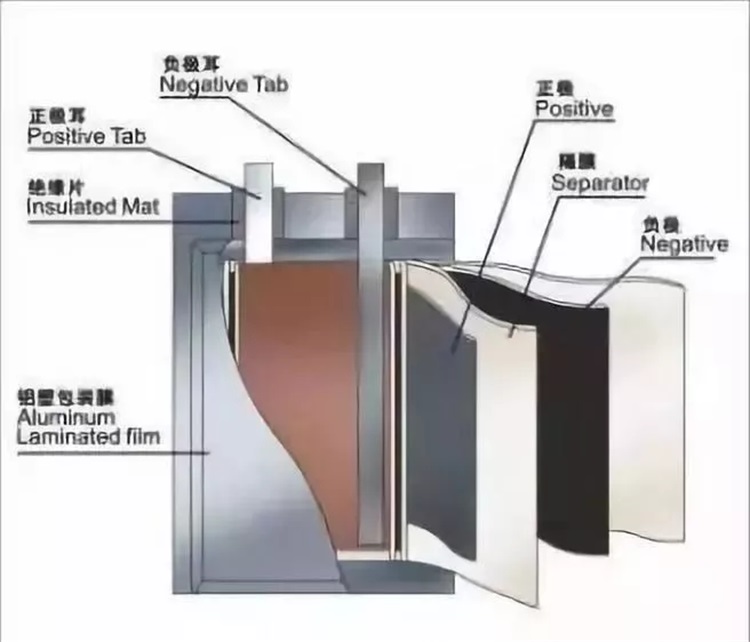
1、鋰電池基本結(jié)構(gòu)
主要材料:正極、負(fù)極、電解液、隔膜
結(jié)構(gòu):圓形、方形;疊片、卷繞
形態(tài):聚合物(軟包裝)、液態(tài)鋰離子(鋼殼)
2、鋰電池工作原理
正極材料:LiMn2O4,負(fù)極材料:石墨
充電時正極的Li+和電解液中的Li+向負(fù)極聚集,得到電子,被還原成Li鑲嵌在負(fù)極的碳素材料中。放電時鑲嵌在負(fù)極碳素材料中的Li失去電子,進(jìn)入電解液,電解液內(nèi)的Li+向正極移動。
3、鋰電池組成原理
①正極構(gòu)造
LiMn2O4(錳酸鋰)+導(dǎo)電劑(乙炔黑)+粘合劑(PVDF)+集流體(鋁箔)正極
②負(fù)極構(gòu)造
石墨+導(dǎo)電劑(乙炔黑)+粘合劑(PVDF)+集流體(銅箔)負(fù)極

4、充電過程
電源給電池充電,此時正極上的電子e從通過外部電路跑到負(fù)極上,正鋰離子Li+從正極“跳進(jìn)”電解液里,“爬過”隔膜上彎彎曲曲的小洞,“游泳”到達(dá)負(fù)極,與早就跑過來的電子結(jié)合在一起。
正極上發(fā)生的反應(yīng)為LiMn2O4 ==Li1-xMn2O4+Xli++Xe(電子)
負(fù)極上發(fā)生的反應(yīng)為6C+XLi+Xe==LixC6

5、放電過程
電池放電,此時負(fù)極上的電子e從通過外部電路跑到正極上,正鋰離子Li+從負(fù)極“跳進(jìn)”電解液里,“爬過”隔膜上彎彎曲曲的小洞,“游泳”到達(dá)正極,與早就跑過來的電子結(jié)合在一起。
正極上發(fā)生的反應(yīng)為Li1-xMn2O4+xli++xe(電子) ==LiMn2O4
負(fù)極上發(fā)生的反應(yīng)為LixC6 == 6C+xLi+xe


